FDA Zulassung
FDA Zulassung: Alles was Sie wissen müssen
Die Food and Drug Administration (FDA) ist eine US-Behörde, die für die Überwachung und Regulierung von Lebensmitteln, Medikamenten, medizinischen Geräten, Tabakprodukten und Kosmetika zuständig ist.
Ihre Hauptaufgabe besteht darin, die öffentliche Gesundheit zu schützen, indem sie dafür sorgt, dass diese Produkte sicher, wirksam und korrekt gekennzeichnet sind. Dies umfasst sowohl inländische als auch importierte Produkte.
Die FDA wurde 1927 gegründet, und ihre Rolle hat sich im Laufe der Zeit weiterentwickelt, insbesondere in Reaktion auf verschiedene medizinische Krisen und Skandale.
O-RINGE SCHNELL UND EINFACH ANFRAGEN?
Nahezu jede Abmessung lieferbar
Angebot in Rekordzeit erhalten
Keine Mindestbestellmengen oder Mindestpositionswerte
Ein Ansprechpartner für alle Anliegen
#1 FDA Zulassung: Grundlagen
Die Zulassung durch die FDA ist ein entscheidender Schritt für die Einführung neuer Medikamente und medizinischer Geräte auf dem US-Markt.
Sie stellt sicher, dass diese Produkte den strengen Sicherheits- und Wirksamkeitsstandards der Behörde entsprechen. Die Zulassung basiert auf einer umfassenden Prüfung der von den Herstellern eingereichten Unterlagen, die die Qualität, Wirksamkeit und Sicherheit der Produkte belegen müssen.
Dies beinhaltet die Durchführung und Bewertung klinischer Studien, die Herstellung nach festgelegten Standards und die Vorlage detaillierter Informationen zur Zusammensetzung und Wirkungsweise des Produkts.
Die FDA-Struktur umfasst verschiedene Zentren und Büros, die sich auf spezifische Produktkategorien spezialisieren, wie zum Beispiel das Zentrum für Arzneimittelbewertung und -forschung und das Zentrum für Lebensmittelsicherheit und angewandte Ernährung.
Diese Struktur ermöglicht es der FDA, auf die spezifischen Herausforderungen und Anforderungen jeder Produktkategorie effektiv zu reagieren.
Das Zulassungsverfahren der FDA ist weltweit bekannt für seine Strenge und Detailliertheit. Die FDA-Zulassung wird oft als Goldstandard in der Pharmaindustrie angesehen, da sie ein hohes Maß an Vertrauen in die Sicherheit und Wirksamkeit eines Produkts signalisiert. Die Entscheidungen der FDA beeinflussen häufig auch die Regulierungspraktiken in anderen Ländern.

#2 FDA Zulassung: Der Zulassungsprozess
Der Zulassungsprozess der Food and Drug Administration (FDA) ist ein komplexer und mehrstufiger Vorgang, der darauf abzielt, die Sicherheit und Wirksamkeit von Medizinprodukten und Arzneimitteln zu gewährleisten, bevor sie auf dem US-Markt zugelassen werden.
Hauptzulassungsverfahren für Medizinprodukte
Die FDA hat verschiedene Zulassungsverfahren für Medizinprodukte, darunter:
- Premarket Notification 510(k) (PMN): Für Produkte, die substantiell äquivalent zu einem bereits existierenden und zugelassenen Produkt sind.
- Premarket Approval (PMA): Dies ist das strengste Verfahren, das für Klasse III Medizinprodukte erforderlich ist. Es beinhaltet eine eingehende Prüfung der Sicherheit und Wirksamkeit durch die FDA.
- Investigational Device Exemption (IDE): Ermöglicht die Verwendung eines Prüfprodukts in klinischen Studien.
- Humanitarian Device Exemption (HDE): Für Geräte, die zur Behandlung oder Diagnose seltener Krankheiten oder Zustände bestimmt sind.
Phasen des Arzneimittelzulassungsverfahrens
Das Zulassungsverfahren für Arzneimittel beinhaltet mehrere Phasen:
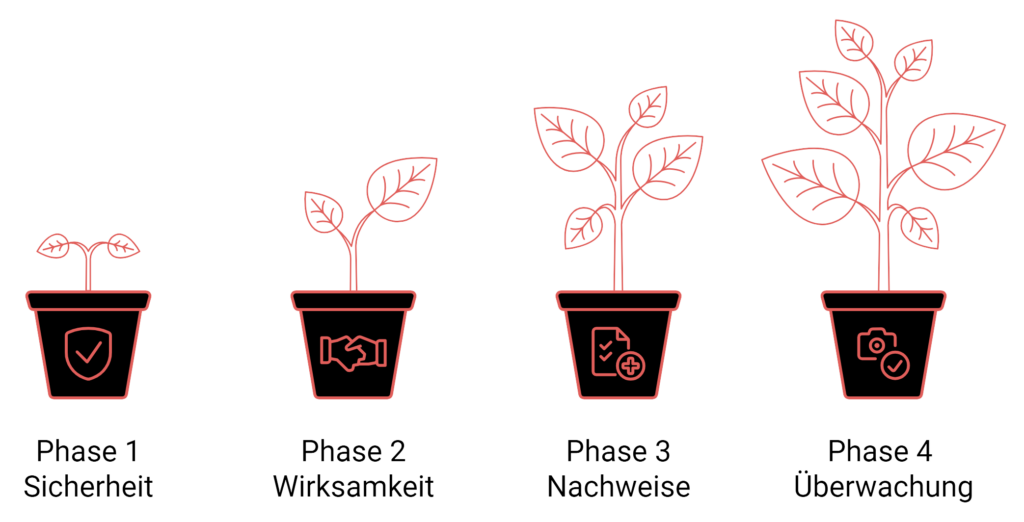
Phase 1: Fokussiert sich auf Sicherheit, umfasst 20 bis 80 gesunde Freiwillige und dauert etwa ein Jahr.
Phase 2: Konzentriert sich auf die Wirksamkeit. In dieser Phase werden ca. 100 bis 300 Patienten über zwei Jahre hinweg beobachtet.
Phase 3: Beginnt, wenn in Phase 2 Wirksamkeitsnachweise erbracht wurden. Sie umfasst mehrere hundert bis 3.000 Patienten und dauert durchschnittlich drei Jahre.
Phase 4: Nachmarktüberwachung zur weiteren Bewertung von Sicherheit und Wirksamkeit nach der Zulassung.
New Drug Application (NDA)
Die Einreichung eines New Drug Application (NDA) ist ein entscheidender Schritt, bei dem der Hersteller die FDA um die Erlaubnis bittet, sein Medikament auf dem US-Markt zu vermarkten. Dieser Antrag umfasst umfangreiche Daten aus Tierversuchen und klinischen Studien sowie Informationen zur Dosierung, Nebenwirkungen und Pharmakokinetik.
Besondere Zulassungsprogramme
Die FDA hat auch spezielle Programme, um die Entwicklung und Überprüfung bestimmter Arzneimittel zu beschleunigen:
- Fast Track: Für Medikamente, die schwerwiegende Erkrankungen behandeln und einen ungedeckten medizinischen Bedarf erfüllen.
- Breakthrough Therapy: Für Medikamente, die eine wesentliche Verbesserung gegenüber bestehenden Behandlungen zeigen.
- Priority Review: Ziel ist es, innerhalb von sechs Monaten über einen Antrag zu entscheiden.
- Accelerated Approval: Kann für vielversprechende Therapien angewandt werden, die eine schwerwiegende oder lebensbedrohliche Erkrankung behandeln.

#3 FDA Zulassung: Herausforderungen und Hürden
Die Food and Drug Administration (FDA) bietet verschiedene Arten von Zulassungen für Medikamente, biologische Produkte und Medizinprodukte an. Zu den gängigen Antragsarten zählen:
New Drug Application (NDA)
Dieser Antrag wird gestellt, wenn ein Unternehmen glaubt, dass es genügend Belege für die Sicherheit und Wirksamkeit eines neuen Medikaments gesammelt hat, um die Anforderungen der FDA für eine Marktzulassung zu erfüllen. Der NDA muss Daten aus verschiedenen technischen Sichtweisen enthalten, darunter Chemie, Pharmakologie, Medizin, Biopharmazie und Statistik.
Abbreviated New Drug Application (ANDA)
Dieser Antrag ermöglicht die Überprüfung und letztendliche Zulassung eines generischen Medikaments. Generische Arzneimittelanträge werden als „abgekürzt“ bezeichnet, da sie normalerweise keine präklinischen (Tier-) und klinischen (menschlichen) Daten zur Sicherheit und Wirksamkeit enthalten müssen. Stattdessen muss der Antragsteller wissenschaftlich nachweisen, dass sein Produkt bioäquivalent (d.h., es wirkt auf die gleiche Weise wie das Innovator-Medikament) ist.
Investigational New Drug Application (IND)
Diese wird benötigt, um eine Ausnahme von der gesetzlichen Anforderung zu erhalten, dass ein Medikament einer genehmigten Marketinganwendung unterliegen muss, bevor es über Staatsgrenzen hinweg transportiert oder verteilt wird.
Biologics License Application (BLA)
Biologische Produkte werden unter den Bestimmungen des Public Health Service (PHS) Act für das Marketing zugelassen. Ein BLA enthält spezifische Informationen über die Herstellungsprozesse, Chemie, Pharmakologie, klinische Pharmakologie und die medizinischen Auswirkungen des biologischen Produkts.
Over-the-Counter Drugs (OTC)
OTC-Arzneimittel können entweder durch einen NDA oder ein OTC-Monographie-Verfahren zugelassen werden. Ein OTC-Monographie-Verfahren ist im Wesentlichen ein „Regelbuch“ für jede therapeutische Kategorie, das Bedingungen wie Wirkstoffe, Anwendungen (Indikationen), Dosierungen, Kennzeichnung und Tests festlegt, unter denen ein OTC-Arzneimittel allgemein als sicher und wirksam anerkannt (GRASE) ist und ohne einen NDA und vorherige FDA-Zulassung vermarktet werden kann.
Für die Zulassung medizinischer Geräte erfolgt ebenfalls ein ähnlicher Prozess wie bei Arzneimitteln. Diese Geräte werden nach Risiko klassifiziert, wobei Klasse I die niedrigste und Klasse III die höchste Risikostufe darstellt.

#4 FDA Zulassung: Elastomere und Code of Federal Regulations (CFR)
Die Bestimmungen des CFR (Code of Federal Regulations) Titel 21 konzentrieren sich insbesondere auf die Vorschriften, die sich auf Elastomere und Gummi im Lebensmittel-, Getränke- und Wassersektor beziehen.
CFR Titel 21 und Elastomere/Gummi
Die FDA-Vorschriften für Gummiprodukte, die in Kontakt mit Lebensmitteln kommen, sind in CFR Titel 21, Kapitel 1, Unterkapitel B, Teil 177, Unterabschnitt C und Paragraph 2600 festgelegt. Diese Vorschriften enthalten Anleitungen zur Herstellung und Verwendung von Elastomeren und Gummi in Produkten, die in der Lebensmittel- und Getränkeindustrie verwendet werden.
Die FDA teilt Lebensmittel in zwei Kategorien ein, wenn es um die Kompatibilität mit Gummi geht:
Klasse I: Diese Kategorie umfasst Lebensmittel wie essbare Öle, Butter, Milch und Milchprodukte sowie Kochöle. Gummiverbindungen, die diesen Anforderungen entsprechen, sind auch mit Lebensmitteln der Klasse II kompatibel.
Klasse II: Diese Kategorie bezieht sich auf Lebensmittel, die keine essbaren Öle oder Milchprodukte enthalten, wie Wasser, alkoholfreie Getränke, alkoholische Getränke und andere wässrige Lösungen.
FDA 21 CFR 177.2600
Die Bestimmung 21 CFR 177.2600 ist im Wesentlichen eine Liste der zugelassenen Basiseleastomere und Vulkanisationsmaterialien.
Diese Materialien werden in der Gummiproduktion verwendet und gelten als sicher. Produkte, die diesen Richtlinien entsprechen, werden in Anwendungen wie Dichtungen, Arbeitsplatten, rutschfesten Pads und Abschirmungen in der Lebensmittelverarbeitung verwendet.
Sie finden sich auch in Metzgereien, pharmazeutischen Verarbeitungsbetrieben, kommerziellen Küchen, Krankenhäusern, Lebensmittelverarbeitungsbetrieben, der Kosmetikindustrie, Industrieanlagen und Lebensmittelgeschäften.
Gängige O-Ring Werkstoffe mit FDA-Zulassung sind FFKM, EPDM, FKM, PTFE, FEP, VMQ UND FVMQ.

#5 FDA Zulassung: Zukunft und Fazit
Die Zukunft des FDA-Zulassungsprozesses sieht einige wichtige Entwicklungen voraus:
Verbesserte Prozesse für die Arzneimittelzulassung und Überwachung
Die FDA hat ihre Prozesse für die Arzneimittelzulassung verbessert, was dazu beiträgt, dass Patienten schnelleren Zugang zu wirksamen Medikamenten erhalten, während das Risiko von Arzneimittelnebenwirkungen minimiert wird.
Neue Gesetze zur Verbesserung des Zulassungsprozesses
Gesetze wie der FDA Safety and Innovation Act (FDASIA) von 2013 wurden erlassen, um den Zulassungsprozess zu verbessern und den Zugang zu neuen Medikamenten zu erweitern.
Erhöhte Effizienz und Kostensenkung
Durch die Verkürzung der mittleren Zulassungszeit für neue molekulare Medikamente von 19 auf 10 Monate und die Einführung neuer Gesetze zielt die FDA darauf ab, den Prozess effizienter zu gestalten
Kontinuierliche Verbesserung und Zusammenarbeit
Die FDA strebt an, ihre Prozesse kontinuierlich zu verbessern und arbeitet dabei mit verschiedenen Organisationen zusammen, um sichere und wirksame Medikamente für Patienten zu entwickeln.
#6 FDA Zulassung: Weitere Fragen beantwortet
Im folgenden Kapitel werden wir weiterführende Fragen zum Thema FDA Zulassung beantworten.
#6.1 FDA Zulassung für Medizinprodukte
Die FDA-Zulassung ist entscheidend für die Sicherheit und Wirksamkeit von Medizinprodukten.
Sie garantiert, dass Produkte strengen Prüfungen unterzogen wurden, bevor sie auf den Markt kommen, was für Patienten und Hersteller gleichermaßen wichtig ist.
#6.2 FDA Zulassung in Deutschland
Auch in Deutschland spielt die FDA-Zulassung eine wichtige Rolle, vor allem für Unternehmen, die ihre Medizinprodukte und Arzneimittel auf dem US-Markt einführen möchten.
Sie symbolisiert hohe Sicherheits- und Qualitätsstandards, was das Vertrauen in diese Produkte stärkt.
„Ich bin überzeugt davon, dass wir unser Wissen mit der Welt teilen sollten. Ich hoffe, dass ich alle Ihre Fragen beantworten konnte. Sollten Sie noch Fragen haben, dann können Sie sich jederzeit gerne bei uns melden. Wir helfen Ihnen gerne weiter.“

Herr der O-Ringe
Autor der Dichtungsakademie
